鯨井智也助教、越後谷健太特任研究員、岸雄介准教授、胡桃坂仁志教授(いずれも定量生命科学研究所)、後藤由季子教授(薬学系研究科)らによる研究グループは、がんタンパク質DEKがゲノムDNAに結合してその構造を変化させ、遺伝子の発現を抑制的に制御する機構を明らかにした。成果は2月21日付で分子生物学の科学誌『Nature Structural & Molecular Biology』に掲載された。
がんタンパク質DEKは、肝臓がんや卵巣がんなどのさまざまながん組織で過剰に存在することが知られており、DEKを過剰に含むがん細胞を持つ患者は治療後の経過が悪いことが知られていた。DEKはクロマチンに多く結合していることが知られていたが、その詳細な機能は不明だった。
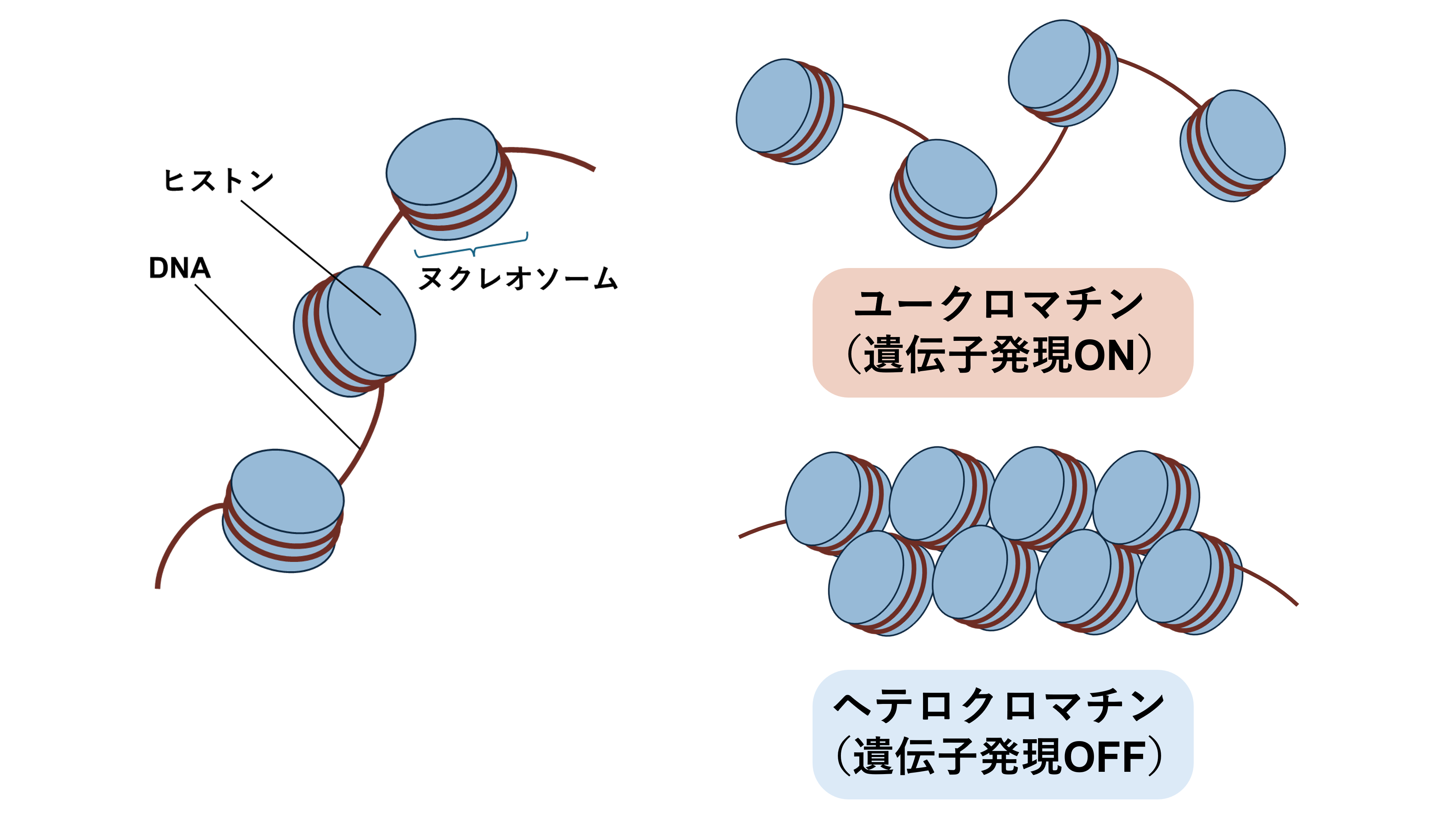
クロマチンは、ヒトを含む真核生物が持つ構造で、ゲノムDNAがヒストンタンパク質に巻き付いたヌクレオソームと呼ばれる構造体が連なって形成されている。クロマチンには、ヌクレオソームが緩んだ状態のユークロマチンと、凝縮された状態のヘテロクロマチンの2状態があり、ヘテロクロマチンでは遺伝子のはたらきが抑制される(図1)。
今回の研究ではまず、DEKがヘテロクロマチンの目印であるヒストンタンパク質のメチル化修飾と共局在していることを確認し、DEKがヘテロクロマチン付近に存在していることが示唆された。さらに試験管内でクロマチンのメチル化実験を行ったところ、DEKによってヒストンタンパク質のメチル化が促進されることが分った。
DEKによるクロマチン構造への影響を調べるために、ヌクレオソームとDEKの構造を解析したところ、二つのヌクレオソームをつなぐリンカーDNAに二つのDEKが結合し、その向きを固定していることが分かった。さらに、DEKを含むポリヌクレオソーム(ヌクレオソームが複数つながった構造体)は、DEKを含まないポリヌクレオソームより小さく、DEKによってクロマチンが凝縮していることが示唆された。
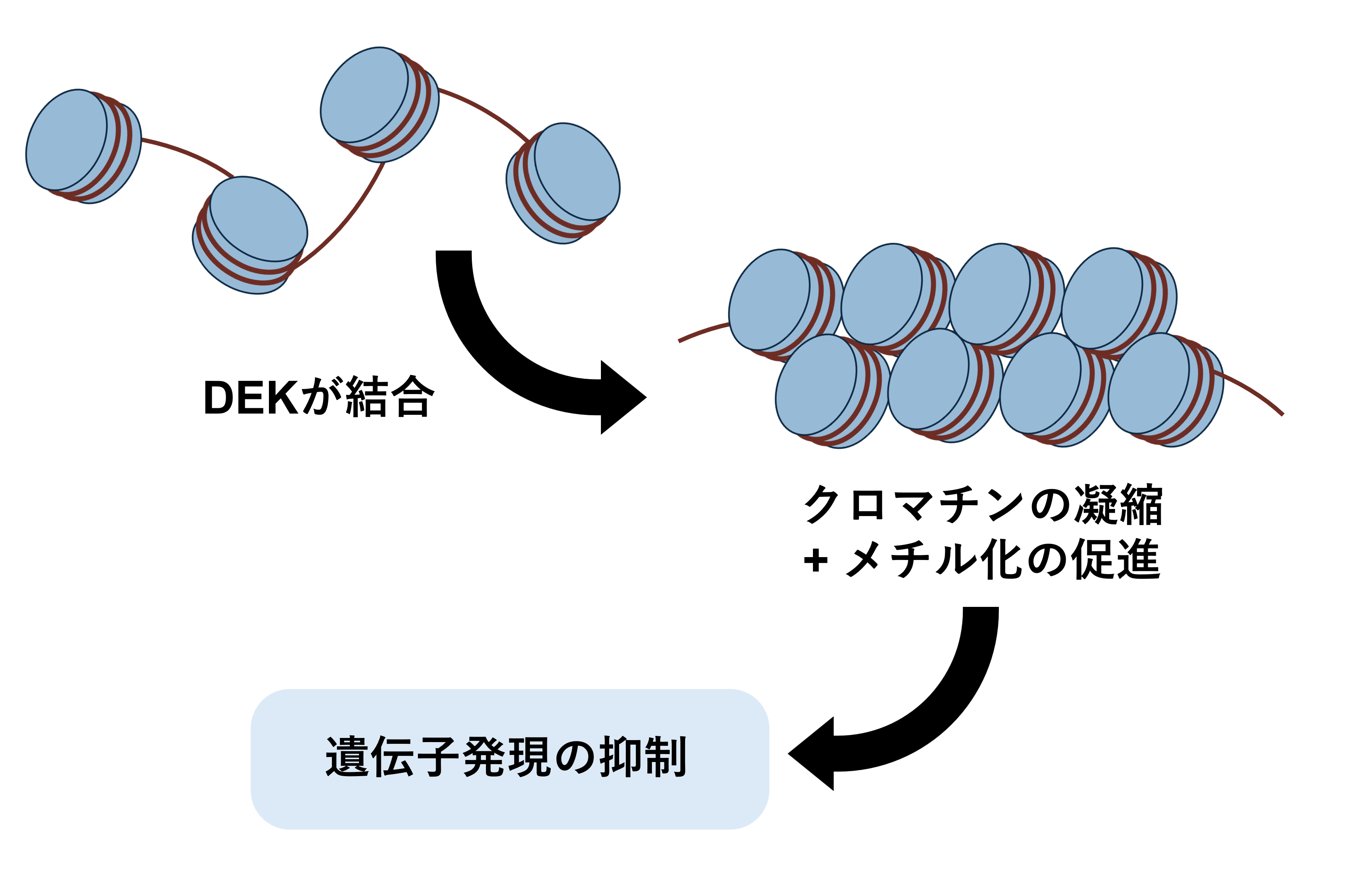
今回の研究によって、DEKがリンカーDNAに結合してクロマチンの凝縮を引き起こし、ヒストンタンパク質のメチル化を促進することで、遺伝子のはたらきを抑制している可能性が示された(図2)。DEKが過剰に存在するがん細胞では、クロマチン構造に異常が生じ、がん細胞特有の遺伝子制御が引き起こされていると考えられる。DEKやクロマチン構造に着目した新たな治療法への応用が期待される。
論文情報
Kujirai, T., Echigoya, K., Kishi, Y., Saeki, M., Ito, T., Kato, J., … & Kurumizaka, H. (2025). Structural insights into how DEK nucleosome binding facilitates H3K27 trimethylation in chromatin. Nature Structural & Molecular Biology, 1-10.
DOI:10.1038/s41594-025-01493-w











