吉見一人講師(東大医科学研究所)、真下知士教授(同研究所)らは、理化学研究所、金沢大学との共同研究で、これまでに国産ゲノム編集技術として開発してきたCRISPR-Cas3が2本鎖DNAを切断する仕組みを世界で初めて解明した。これにより技術改良が容易になり、医療や産業分野への利用が期待される。成果は8月29日付の国際科学雑誌『Nature Communications』オンライン版で公開された。
CRISPR-Casシステムは、多くの細菌が持っている免疫防御システムで、DNAを人工的に切断できる。2020年度ノーベル化学賞の授賞理由となり、現在も世界中で利用されているCRISPR-Cas9と違い、CRISPR-Cas3は大きくゲノムを削る特徴を持ち、狙ったゲノム配列以外への影響も低い。そこで安全で確実に遺伝子を破壊できる国産ゲノム編集技術として開発されてきた。ゲノム編集では狙ったゲノム部位の2本鎖DNAの両方の鎖を切る必要があるが、CRISPR-Cas3はその機能を持つ「ヌクレアーゼドメイン」を一つしか持っておらず、2本鎖DNAを切断するメカニズムは不明だった。
研究では、CRISPR-Cas3は狙った場所の2本鎖DNAをほどいて片方の鎖を手繰り寄せながら、1本鎖DNAをそれぞれ別々に切ることを発見し、その過程を高速原子間力顕微鏡で撮影することに成功した。
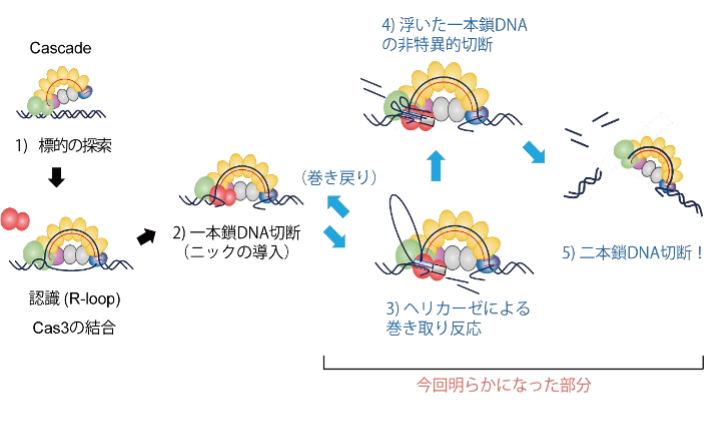
この研究はCRISPR-Cas3の精度・効率を向上させる上で重要な知見となり、既存のゲノム編集技術より安全性の高い国産ゲノム編集技術として広い分野で応用が期待される。











